Die gelgefüllten Mammaimplantate / Brustimplantate Impleo™ stammen von GCA (GC Aesthetics).
Gelgefüllte Brustimplantate sind zur Verwendung bei vergrößernder kosmetischer Mammaplastik oder bei Brustrekonstruktion entwickelt. Sie sind in runden und in anatomischen Formen erhältlich. Die Silikon-Elastomerdichtung kann sowohl glatt als auch mit einer äußeren Oberflächentextur produziert werden, um einen störungsfreien Kontakt für die Kollagenoberfläche zu bieten. Sie sind mit einem kohäsiven oder hochkohäsiven Gel gefüllt. Jedes gelgefüllte Brustimplantat wird in einer Kartonschachtel geliefert und ist in einer versiegelten doppelten Primärverpackung verpackt. Die Verpackung enthält außerdem abtrennbare Etiketten, auf denen die Merkmale des Implantats (Chargennummer, Artikelnummer) angegeben sind.
INDIKATIONEN
Diese gelgefüllten Brustimplantate sind für die folgenden Verfahren indiziert:
- Kosmetische Augmentationsplastik.
- Augmentation und Korrektur der Körperkontur bei kongenitalen Fehlbildungen der Brust.
- Rekonstruktion der Brust nach subkutaner Mastektomie und anderen in Frage kommenden Mastektomie-Eingriffen oder Traumen. · Kombinierte Fehlbildungen der Brust und Thoraxwand.
- Auswechslung von Vorrichtungen aus medizinischen und kosmetischen Gründen.
KONTRAINDIKATIONEN
Die Verwendung der Implantats ist bei Patientinnen kontraindiziert, die an einer oder mehreren der folgenden Erkrankungen oder Zustände leiden:
- FIBROZYSTISCHE Erkrankung.
- UNGENÜGENDE GEWEBEDECKUNG aufgrund von Strahlenschädigung der Thoraxwand, enge Thoraxhauttransplantate oder radikale Resektion des M. pectoralis major.
- BESTEHENDES LOKALES ODER METASTATISCHES MAMMAKARZINOM.
- Geschwächtes Immunsystem/Immunsuppression.
- Anamnese mit Sensibilität gegenüber Fremdkörpern oder Atopie.
- UNBEFRIEDIGENDE ANAMNESE in bezug auf Augmentation/Rekonstruktion.
- Mangelnde PHYSIOLOGISCHE/PSYCHOLOGISCHE Eignung der Patientin.
- AKTIVE INFEKTION eines Körperbereichs.
- Kürzere Zeit zurückliegender Mammaabszeß.
- Anamnestisch schlechte Wundheilung.
- Andere ernsthafte Erkrankungen, die nach Meinung des Chirurgen die Gesundheit des Patienten beeinträchtigen könnten.
- Da keine Daten bezüglich der Verwendung dieser Produkte in Verbindung mit Dermal Fillern vorliegen, ist die Verwendung von Dermal Fillern in der Nähe dieser Produkte (z.B. im Hautareal des Dekolletés) kontraindiziert. Ärzte sollten ihren Patienten ebenfalls von der weiteren Verwendung von Dermal Fillern in der Nähe dieser Produkte abraten.
- Diese Produkte sind nicht für die Behandlung von Kindern, schwangeren oder stillenden Frauen vorgesehen.
Wichtig: Es ist liegt in der VERANTWORTUNG des CHIRURGEN, die Eignung der Patientin für eine Implantation zu beurteilen und die Operationstechnik zu wählen, die sowohl für die Patientin als auch für den gewählten Implantatstyp/-design geeignet ist.
INFORMATION FÜR PATIENTEN
Jeder chirurgische Eingriff ist potenziell mit Komplikationen und Risiken verbunden. Man weiß, dass Operationen zum Einsetzen von Brustimplantaten den Patienten aus psychologischer Sicht Befriedigung verschaffen, aber wie bei jedem anderen chirurgischen Eingriff auch können Komplikationen und Risiken auftreten. Der Einsatz eines Brustimplantats ist ein elektiver Eingriff, und die Patienten sollten vom Chirurgen zum Verhältnis zwischen den damit verbundenen Risiken und Vorteilen angemessen beraten werden. Jede mögliche Komplikation und alle Warnhinweise sollten mit den Patienten besprochen werden, bevor sich diese für die Operation entscheiden.
Während des Erstgesprächs sollte allen Patienten die Patienten-Informationsbroschüre ausgehändigt werden, damit sie genug Zeit haben, um die Risikohinweise, die Empfehlungen zur Nachsorge und die Informationen zu den mit den Brustimplantaten verbundenen Vorteilen durchzulesen und zu verstehen, um eine fundierte Entscheidung über die Operation treffen zu können. Das Patientenhandbuch enthält außerdem ein Zustimmungsformular (Patient Informed Consent Form), mit dessen Hilfe die Patienten Kopien der Implantatdaten (z. B. die Chargennummer) für ihre Unterlagen aufbewahren können. Dieses Dokument ist im PDF-Format auf unserer Internetseite www.gcaesthetics.com/we-care/ verfügbar.
LEBENSDAUER
Die Patientinnen müssen darüber informiert werden, dass Brustimplantate nicht als Einsätze betrachtet werden sollten, die ein Leben lang behalten werden können. Dafür sprechen eine Reihe von Gründen, einschließlich der potenziell unterschiedlichen physiologischen Reaktionen und Implantationsverfahren, der inhärenten Eigenschaften des Designs von Silikonimplantaten sowie externe, mechanisch bedingte Einflüsse. Es sollte immer davon ausgegangen werden, dass die Implantate während der Lebensdauer der Patientin eventuell entfernt oder ersetzt werden müssen und deshalb eine erneute Operation notwendig wird. In der veröffentlichten Literatur wird jedoch davon berichtet, dass glatte Brustimplantate zwischen 10 und 20 Jahren halten können. Aus diesem Grund wird davon ausgegangen, dass diese glatten Brustimplantate eine ähnliche Lebensdauer wie in der veröffentlichten Literatur beschrieben (schätzungsweise 10-20 Jahre) haben werden, wenn sie wie vorgeschrieben implantiert und unter normalen Bedingungen verwendet werden.
Anhand klinischer Untersuchungen zu den texturierten gelgefüllten Implantaten von GC Aesthetics wurde festgestellt, dass die Implantate beim derzeitigen Stand der Wissenschaft nach 10 Jahren eine Haltbarkeit von 82,4 % aufweisen (erneute Operationen waren bei 17,6 % der Implantate notwendig, die ursprünglich eingesetzt wurden). Darüber hinaus wird GC Aesthetics eine klinische Langzeitstudie über seine glatten Brustimplantate durchführen, um kurz- und langfristige Sicherheits- und Leistungsdaten sowie Überlebensdaten über eine Dauer von 10 Jahren zu sammeln.
MRT-Kompatibilität
Anmerkung: Obwohl diese Implantate nicht speziell auf die Kompatibilität mit einer MRT getestet wurden, möchten wir darauf hinweisen, dass alle aus medizinisch für Implantate geeignetem Silikonmaterial hergestellt wurden, das mit MRT-Scans kompatibel ist Das Silikon-Implantatmaterial ist dasselbe, das auch für andere Silikonimplantate verwendet wird, mit denen sich Patienten bereits einem MRT-Scan unterzogen haben, ohne dass bisher Kompatibilitätsprobleme gemeldet wurden.
VERWENDUNG VON STEROIDEN
Die Patientin sollte einen Arzt konsultieren, bevor sie an der Implantationsstelle Steroid-Medikamente verwendet, um eine Extrusion des Implantats zu verhindern.
WARNHINWEISE
VERÄNDERUNG DER IMPLANTATE
An den Mammaprothesen dürfen vor der Implantation keine Veränderungen vorgenommen werden. Eine Veränderung der Implantate führt zum Erlöschen aller ausdrücklichen oder impliziten Garantien.
BESCHÄDIGUNG DES IMPLANTATS – BESCHÄDIGUNG WÄHREND DER OPERATION
Besondere Vorsicht gilt beim Gebrauch und der Handhabung der Implantate, um das Risiko einer Beschädigung der Hülle zu minimieren. Alle Implantate werden unter bekannten Herstellungstechniken sowie strikten Qualitätsstandards produziert, dennoch kann es zum Bruch einiger Implantate beim Gebrauch oder der Handhabung kommen, sowohl bei der Erst-Operation wie auch bei allen folgenden.
Es muss besonders darauf geachtet werden, dass es während der Implantations- oder Explantationsoperation zu keinen unbeabsichtigten Schäden kommt.
– Das Implantat darf nicht in Kontakt mit scharfen chirurgischen Instrumenten, wie Skalpellen, Zangen, Gefäßklemmen, Nähnadeln oder Subkutannadeln, gelangen.
– Das Implantat darf nicht in Kontakt mit stumpfen chirurgischen Instrumenten, wie Klemmen, Spreizern und Dissektoren, gelangen.
– Das Implantat darf nicht in Kontakt mit Kauterisationsgeräten gelangen.
– Es darf zu keiner übermäßigen Manipulation, Krafteinwirkung oder Beanspruchung kommen.
Vor dem Gebrauch müssen die Implantate sorgfältig auf intakten Aufbau überprüft werden. Geschädigte Produkte dürfen nicht implantiert werden, versuchen Sie nicht, das beschädigte Produkt zu reparieren. Zum Zeitpunkt der Operation sollte ein zweites Implantat im Falle von Schäden oder Verunreinigungen am ersten Implantat vorhanden sein. Die empfohlenen Vorgehensweisen zum Testen, Untersuchen und der Handhabung der Produkte sollten sorgfältig befolgt werden, um eine korrekte Verwendung des Implantats zu gewährleisten. Patienten müssen angewiesen werden, andere behandelnde Ärzte auf das Vorhandensein von Implantaten hinzuweisen, um das Risiko der Beschädigung möglichst gering zu halten.
INTERFERENZEN IM MAMMOGRAMM
Bei der herkömmlichen Plazierung der Brust zur Mammographie können nach der Augmentationsplastik erhebliche Einschränkungen auftreten. Das Implantat kann die mammographische Erkennung von Mammakarzinomen im Frühstadium behindern, da es das darunterliegende Brustgewebe verdecken bzw. das darüberliegende Gewebe komprimieren und damit verdächtige Läsionen in der Brust verschleiern kann. Die Patientinnen sollten angewiesen werden, sich zur Untersuchung in die Hand eines Radiologen zu begeben, der Erfahrung in den neuesten Techniken und Geräten für die Mammographie mit Brustprothesen besitzt, und ihn auf Vorliegen, Art und Position der Implantate hinzuweisen. Bei anatomisch geformten Implantaten ist außerdem auf die Ausrichtungsmarkierungen zu achten.
EINMALIGER GEBRAUCH
Die Prothesen sind zum EINMALIGEN GEBRAUCH BESTIMMT. EXPLANTIERTE PROTHESEN DÜRFEN NICHT WIEDERVERWENDET ODER RESTERILISIERT WERDEN. Explantierte Prothesen sollten nicht wiederverwendet werden, da durch die erneute Reinigung und Sterilisierung keine ausreichende Entfernung von biologischen Rückständen wie Blut, Gewebe und anderen Substanzen gewährleistet ist, die resistente Erreger enthalten können.
VERWENDUNG VON MEDIKAMENTEN
Nagor kann keine Sicherheitsprognose oder -garantie geben, wenn Arzneimittel wie z.B. Anästhetika, Steroide, Antibiotika oder Vitaminlösungen in das Prothesenlumen eingebracht werden. Vor einer solchen Einbringung ist der Hersteller des Arzneimittels zu konsultieren.
MÖGLICHE KOMPLIKATIONEN
Folgende mögliche Komplikationen können in Verbindung mit den Gelimplantate auftreten:
Weitere mögliche Komplikationen, die bei allen chirurgischen Eingriffen auftreten können, sollten ebenfalls mit der Patientin besprochen werden. Hierzu gehören, wenngleich nicht ausschließlich:
- Infektionen (siehe unten)
- Hämatome (siehe unten)
- starke Flüssigkeitsansammlungen (siehe unten)
- Gefühlsverlust (siehe unten)
- Reaktion auf Medikamente
- Nervenschädigung
- Abstoßung des Fremdimplantats
- schlechte Wundheilung.
VERSEHENTLICHE RUPTUR DES IMPLANTATS IN DER ROTHESENTASCHE
Bei einer versehentlichen Ruptur kann die Gelmasse mit dem Zeigefinger einer Hand, über die zwei Paar Handschuhe gezogen wurden, penetriert werden, während mit der anderen Hand Druck auf die Brust ausgeübt wird. Das Gel kann in der Hand aus der Tasche herausmanipuliert werden; danach wird der äußere Handschuh zur Entsorgung über die Gelmasse gezogen. Die Prothesentasche mit Gazetupfern austupfen. Isopropylalkohol hilft beim Reinigen der Instrumente von dem Gel.
BRUSTIMPLANTAT-ASSOZIIERTES ANAPLASTISCHES GROßZELLIGES LYMPHOM (BIA-ALCL)
In Sicherheitshinweisen für Europa, Dokumenten der amerikanischen Arzneimittelaufsicht FDA und aktuellen wissenschaftlichen Studien wird auf einen möglichen Zusammenhang zwischen Brustimplantaten und dem seltenen Auftreten anaplastischer großzelliger Lymphome (ALCL), einer Unterart der Hodgkin-Lymphome, hingewiesen. Frauen mit texturierten Brustimplantaten haben demnach möglicherweise ein geringes, jedoch höheres Risiko, an einem ALCL im Gewebe in Implantatnähe zu erkranken. Dieser Sachverhalt wird in der WHO-Klassifizierung 2016 unter dem Begriff „ALCL – AIM“ geführt. In diesen Sicherheitsberichten wird von einer sehr kleinen Zahl Fälle in der Flüssigkeit oder im Narbengewebe um Implantate herum berichtet.
Die Hauptsymptome, die bei Frauen mit BIA-ALCL und Brustimplantaten auftraten, sind langanhaltende Schwellungen oder Schmerzen, spät auftretende und langfristig feststellbare Serome5, Kapselkontraktur oder eine Masse in der Implantatumgebung. Sollten Frauen an den oben beschriebenen Symptomen leiden oder ein Verdacht auf BIA-ALCL bestehen, wird empfohlen, die Patientinnen zu untersuchen, um ein ALCL in Implantatnähe auszuschließen. Entsprechend den empfohlenen Richtlinien sollten für die Untersuchung auf BIA-ALCL frische Seromflüssigkeit sowie repräsentative Proben der Kapsel entnommen und diese zur pathologischen Untersuchung geschickt werden, um eine ALCL-Erkrankung auszuschließen. Für die Diagnose sollte eine zytologische Untersuchung der Seromflüssigkeit unter Zuhilfenahme eines Ausstrichs mit Wright-Giemsa-Färbung und Zellblock-Immunhistochemie durchgeführt werden, bei der nach einem Cluster of Differentiation (CD) und Markern für anaplastische Lymphomkinase (ALK) gesucht wird. Meist wird ein durch Brustimplantate verursachtes ALCL durch Explantation des Implantats sowie der umliegenden Kapsel behandelt, es wurden in der Vergangenheit aber auch Behandlungen mit Chemotherapie und Bestrahlung durchgeführt.
Sollte eine Ihrer Patientinnen an BIA-ALCL erkranken, wenden Sie sich unter folgender E-Mail-Adresse an den Hersteller: ukvigilance@gcaesthetics.com. Individuelle Behandlungsregimes sollten von einem disziplinübergreifenden Ärzteteam aufgestellt werden.
„BREAST IMPLANT ILLNESS“
Ein kleiner Anteil der Frauen, die sich aus ästhetischen oder rekonstruktiven Gründen für Brustimplantate entscheiden, gibt an, an einer Reihe von Symptomen zu leiden, die ihrer Überzeugung nach durch das Vorhandensein der Brustimplantate hervorgerufen werden. Es handelt sich hierbei um keine medizinische Diagnose, die Symptome werden aber unter „Breast Implant Illness“ (Brustimplantatkrankheit, BII) zusammengefasst.
Diese verschiedenen allgemeinen Symptome sind äußerst vielfältig, und alle Fälle sind selbstdiagnostiziert und selbstberichtet. Zu den Symptomen gehören, ohne darauf beschränkt zu sein, grippeähnliche Symptome wie extreme Müdigkeit, Gehirnnebel, Gelenkschmerzen, mit dem Immunsystem zusammenhängende Symptome, Schlafstörungen, Depressionen, hormonelle Störungen, Kopfschmerzen, Haarausfall und Schüttelfrost.
Es gibt eine Reihe von anderen Gründen, die für diese Symptome verantwortlich sein könnten, darunter Hintergrunderkrankungen oder hormonelle Umstellungen. Darüber hinaus gibt es eine Reihe wissenschaftlicher Studien, die ähnliche Symptome untersuchen, die bei Frauen der Allgemeinbevölkerung sowohl mit als auch ohne Brustimplantate auftreten. Etwa 50 % der Frauen, die „BII“ bei sich erkennen, melden nach Entfernen des Implantats eine Verbesserung der Symptome, die manchmal vorübergehend und manchmal dauerhaft ist. Es scheint daher, dass durch Entfernen der Brustimplantate nicht zwangsläufig bei allen Betroffenen die Symptome verbessert werden. Zum jetzigen Zeitpunkt gibt es keine Forschungsergebnisse, die darauf schließen lassen, welche Symptome durch Entfernen eines Brustimplantats verbessert werden und welche nicht.
Es gibt aktuell keine Tests zur Bestätigung von „BII“. Die Forschung auf diesem Gebiet wird fortgesetzt, insbesondere an Patientinnen mit einer Autoimmunerkrankung oder einer Veranlagung zu Autoimmunerkrankungen. Brustimplantate sind bei Frauen mit geschwächtem Immunsystem oder Immunsuppression kontraindiziert – siehe Abschnitt KONTRAINDIKATIONEN oben. Wenn eine Patientin vermutet, dass sie an „BII“ leidet, sollte sie sich medizinisch beraten lassen. Ihre Symptome sind möglicherweise nicht auf die Implantate zurückzuführen. In dem Fall sollten andere medizinische Untersuchungen nicht ausgelassen werden, um die Ursache der Symptome herauszufinden.
ASYMMETRIE
Zur Asymmetrie von Brustimplantaten kann es durch ungeeignete Erstplazierung, Verlagerung oder durch unterbliebene Korrektur einer vorbestehenden Asymmetrie durch individuelle Variation der Prothesengröße kommen. Vorbestehende Asymmetrien lassen sich nicht immer vollkommen korrigieren. Asymmetrien können auch ein Anzeichen für Kapselkontraktur, Flüssigkeitsansammlungen, Infektionen, postoperative Dysplasie der Brust, einseitig unterschiedliche Muskelentwicklung oder Deflation sein und bedürfen der weiteren Untersuchung.
KALKDEPOSITION
Die Verkalkung des Brustgewebes mit zunehmendem Alter ist ein natürlicher Vorgang, der unabhängig vom Vorliegen einer Prothese stattfindet. Verkalkungen des Brustgewebes können auch nach der Implantation von Fremdkörpern auftreten; die Ursache hierfür ist nicht geklärt, und die Zahl der berichteten Fälle ist gering. Mikrokalzifikationen treten nach Implantationen normalerweise an der oder rund um die fibröse Kapsel auf und haben die Form von dünnen Plaques oder Kalkansammlungen. Stärkere Mikrokalzifikationen können zur Verhärtung der Brust und zu Unbehagen führen und erfordern unter Umständen einen chirurgischen Eingriff.
KAPSELKONTRAKTUR
Die Kapselfibrose ist eine häufige Komplikation bei Mammaimplantaten. Die Bildung einer fibrösen Gewebekapsel rund um die Prothese ist eine normale physiologische Reaktion auf den Fremdkörper; nicht bei allen Kapseln kommt es zur Kontraktur. Die Kontraktur des fibrösen Kapselgewebes rund um das Implantat kann zu Verhärtungen, Unbehagen und Schmerzen in der Brust, Verformung der Brust, Tastbarkeit des Implantats oder zur Verlagerung der Implantats führen. Die Ursache der Kapselkontraktur ist unklar, hier dürften jedoch verschiedene Faktoren eine Rolle spielen. Die Kapselfibrosen können unterschiedlich stark ausgeprägt sein und ein- oder beidseitig innerhalb von Wochen oder Jahren nach der Operation auftreten. In schweren Fällen ist unter Umständen eine chirurgische Intervention erforderlich. Nach der Kapseleröffnung oder -entfernung kann eine erneute Kapselfibrose auftreten. Knoten, die mit kapsulären Narbenbildungen verwechselt werden, können die Diagnose eines tastbaren Tumors verzögern. Im Zweifelsfall müssen Knoten daher unverzüglich untersucht werden.
VERZÖGERTE WUNDHEILUNG
Bei einigen Patienten tritt eine verzögerte Wundheilung auf, bei anderen verheilt die Inzisionsstelle möglicherweise schlecht. Unter Umständen kann sie sich aufgrund einer Verletzung oder Infektion wieder öffnen. Sollte das Implantat freiliegen, muss erneut operiert werden. Gewebsnekrose ist das Absterben von Gewebe um das Implantat. Sie führt zu einer verzögerten Heilung, kann zu Wundinfektionen beitragen und macht unter Umständen eine operative Korrektur und/oder eine Explantation notwendig. Gewebsnekrose trat in der Vergangenheit nach der Behandlung mit Steroiden, Chemotherapie, Strahlentherapie von Brustgewebe und bei Rauchern auf, kann jedoch auch ohne eindeutige Ursache auftreten.
EXTERNE KAPSELERÖFFNUNG
Eine manuelle Sprengung der verhärteten Kapsel von außen kann zur Schwächung oder zum Defekt der Hülle führen. Rupturen wurden mehrfach berichtet. Nagor rät daher von einer externen Kapseleröffnung ab und übernimmt keine Verantwortung für die Unversehrtheit des Implantats, wenn manuelle Kompressions- oder andere Techniken mit externer Krafteinwirkung verwendet werden.
UNZUFRIEDENHEIT MIT DEM ERGEBNIS
Die Wahl der falschen Prothesengröße, eine ungeeignete Narbenposition, hypertrophes Narbengewebe sind meist mit der Operationstechnik assoziiert. Die sorgfältige Auswahl der richtigen Prothesengröße, die Schaffung einer hinreichend großen, passenden Prothesentasche und die Wahl einer aktuellen, akzeptablen Operationstechnik liegen in der Verantwortung des Chirurgen.
VERLAGERUNG DES IMPLANTATS
Implantate können sich verlagern; die Folgen sind Unbehagen bzw. eine Verformung der Brust. Die Gefahr einer Verlagerung erhöht sich durch die Verwendung schwieriger Plazierungstechniken, bei denen eine relativ kleine Prothesentasche verwendet wird und die Genauigkeit der Plazierung eingeschränkt ist. Bei Verlagerung der Prothese ist eine operative Korrektur erforderlich.
ERKLÄRUNG VON MAMMAPROTHESEN
Wenngleich hierzu keine definitiven Berichte in der ärztlichen Fachliteratur vorliegen, ist davon auszugehen, daß viele Mammaprothesen zu einem späteren Zeitpunkt chirurgisch explantiert oder ausgewechselt werden müssen. Dies ist auch bei vielen anderen chirurgischen Prothesen der Fall, die häufig erneuert werden müssen, um die fortgesetzte Zufriedenheit des Patienten zu gewährleisten. Wegen der sehr verschiedenen körperlichen Reaktionen der Patientinnen auf Brustimplantate, Unterschieden in der Operationstechnik und der ärztlichen Behandlung und möglichen Komplikationen sollten die Patientinnen darauf hingewiesen werden, daß die Prothesen nicht als lebenslange Implantate betrachtet werden sollten und daß eine chirurgische Explantation jederzeit nötig werden kann. Nagor übernimmt keine Garantie für die Implantationsdauer der Vorrichtung.
EXTRUSION
Eine instabile oder beeinträchtigte Gewebedeckung bzw. Unterbrechung der Wundheilung kann zur Exposition und Extrusion des Implantats führen. Zu den Ursachen bzw. Einflußfaktoren gehören Infektionen, Wunddehiszenz, infektiöse oder nichtinfektiöse Nekrose, Kapselkontraktur, externe Kapseleröffnung, ungeeigneter Hautlappen, falsche Größe und Plazierung des Implantats bzw. Gewebeerosion durch Falten in der Prothese. Extrusionen treten vermehrt dann auf, wenn die Prothese in Verletzungsgebieten implantiert wurden: in vernarbtem, stark bestrahltem oder verbranntem Gewebe oder Gebieten mit Knochentrümmern; wenn im Implantationsgebiet eine starke chirurgische Reduktion vorgenommen wurde; und bei Einbringung von Steroiden in die Prothesentasche.
GRANULOM
Die Entstehung von Granulomen ist eine bekannte Gewebsreaktion auf das Vorhandensein von Fremdkörpern. Es ist möglich, dass körpereigenes Gewebe auf das Implantat reagiert und Silikongranulome ausbildet.
HÄMATOME/FRÜHE SEROME
Hämatome und seröse Flüssigkeitsansammlungen sind Komplikationen, die bei jedem invasiven Eingriff auftreten können. Postoperative Hämatome und frühe Serome6 können zu Infektionen bzw. zur Kapselkontraktur beitragen. Die Gefahr von postoperativen Hämatomen und Seromen lässt sich durch sorgfältige Hämostase während der Operation und durch eventuelle postoperative Verwendung eines geschlossenen Dränagesystems verringern. Übermäßige persistierende Blutungen müssen vor Implantation der Vorrichtung gestillt werden. Eine postoperative Evakuierung von Hämatomen und Seromen muss vorsichtig erfolgen, um eine Kontamination oder Beschädigung des Implantats zu vermeiden.
FALSCHE LAGE UND ROTATION DES ANATOMISCHEN IMPLANTATS IN DER IMPLANTATTASCHE
Eine falsche Lage oder Rotation des anatomischen Implantats kann vorkommen, wenn die Implantattasche zu groß ist. Bei der Präparation der Implantattasche für ein anatomisches Implantat muss daher besonders sorgfältig vorgegangen werden.
INFEKTION
Vorbestehende Infektionen, die nicht vor der Implantation der Implantats behandelt werden, erhöhen das Risiko einer periprosthetischen Infektion. Darauf achten, daß das Implantat und Füllzubehör nicht mit Kontaminanzien in Kontakt kommen, die das Infektionsrisiko erhöhen. Infektionen stellen bei jedem invasiven Eingriff ein Risiko dar. Infektionen im Bereich von Mammaprothesen können Tage, Wochen oder sogar Jahre nach der Operation auftreten. Zu den berichteten Anzeichen einer akuten Infektion bei Mammaprothesen gehören Erytheme, Berührungsschmerzhaftigkeit, Flüssigkeitsansammlungen, Schmerzen und Fieber. Die Zeichen einer subklinischen Infektion sind möglicherweise nur schwer erkennbar. Postoperative Infektionen sollten nach allgemeiner
medizinischer Praxis aggressiv behandelt werden, um schwerere Komplikationen zu vermeiden. Bei therapieresistenten oder nekrotisierenden Infektionen ist unter Umständen eine Entfernung des Implantats erforderlich. Kapselkontrakturen können mit einer Infektion im Prothesenumfeld assoziiert sein.
SCHMERZEN
Schmerzen unbekannter Genese, die nicht mit den hier beschriebenen Komplikationen in Zusammenhang stehen, bedürfen der umgehenden Untersuchung.
OBERFLÄCHLICHE PHLEBITIS
In seltenen Fällen kann es während des Einsetzens des Brustimplantats zu Schäden an den Venenwänden kommen. Dies kann zu einer oberflächlichen Phlebitis führen, also der Entzündung der Venen durch ein Blutgerinnsel direkt unterhalb der Hautoberfläche. Diese Komplikation ist nur selten ernsthaft und wird mit der richtigen Behandlung für gewöhnlich schnell behoben.
PTOSIS
Ptosis oder das Herabhängen der Brust ist eine Deformität, die vor und nach einer Brustoperation auftreten kann. Vor der Brustoperation können sich Zeit und Schwerkraft auf die natürliche Brust auswirken, da sie weder über Knochen noch Knorpel verfügt, und es kann zu einer Überdehnung der Drüsen und Haut kommen. Nach der Brustoperation können sich Größe, Gewicht und Position der Brustimplantate auf das Ausmaß der Ptosis auswirken. In schweren Fällen kann diese Komplikation häufig eine Reintervention erforderlich machen.
RUPTUR VON GELIMPLANTATE
Zur postoperativen Ruptur der Gelimplantate kann es kommen, wenn das Implantat bei der Handhabung oder während der Operation beschädigt wurde. Kontraktur, Trauma oder übermäßige Manipulation können ebenfalls zur Ruptur führen. Rupturen unbekannter Ursache wurden ebenfalls berichtet. Wegen der kohäsiven Eigenschaften des Gels kann es vorkommen, daß Gelrupturen unbemerkt bleiben, bis eine Operation aus anderen Gründen (z.B. Größenwechsel) vorgenommen wird. Trotz der Kohäsivität des Gels kann es unter Druck zum Austritt des Gels aus der Prothesentasche kommen. In diesem Fall ist unter Umständen ein weiterer chirurgischer Eingriff erforderlich, um das Gel zu bergen. Über Entzündungen und die Bildung von Silikongranulomen wurde berichtet. Wenn Verdacht auf eine Hüllenruptur besteht, muss das Implantat entfernt werden.
GEFÜHLSSENSATION
Das Risiko einer zeitweisen oder dauerhaften Dysästhesie besteht bei jedem invasiven Eingriff. Durch eine umsichtige Operationstechnik kann dieses Risiko verringert, jedoch nicht ausgeschaltet werden. Über eine zeitweise oder dauerhafte Dysäthesie im Mamillen-/Areolenbereich und in selteneren Fällen in der gesamten Brust nach Implantationen wurde berichtet. Die Gefahr von neurologischen Schäden nimmt mit umfangreicheren Eingriffen zu.
Implantierte Mammaprothesen können die Stillfähigkeit behindern. Die eigentliche Ursache hierfür kann jedoch auch die vorangegangene Rekonstruktion der Brust sein.
LYMPHÖDEM DER OBEREN EXTREMITÄT
Ein Lymphödem ist eine chronische Erkrankung, die sich durch Anschwellen des Armes, der Hand oder der Brust auszeichnet. Dieses Anschwellen kann bei Brustkrebsbehandlungen aufgrund der Ansammlung von Lymphflüssigkeit im interstitiellen Gewebe entstehen. Diese Erkrankung schränkt die Lebensqualität aufgrund des veränderten Körperbilds, der eingeschränkten Armfunktion und dem höheren Risiko für andere Komplikationen, einschließlich Infektionen und Cellulitis, bekanntermaßen stark ein.
Aktuelle Studien legen nahe, dass eine Sofortrekonstruktion der Brust mit einem niedrigeren Risiko für nach Mastektomie entstehendes Lymphödem in Verbindung steht. Zu den Behandlungsoptionen gehört die konservative Behandlung oder ein supermikrochirurgischer Eingriff. Es ist jedoch keine vollständige Heilung für Lymphödeme bekannt.
FÄLTCHEN – UND FALTENBILDUNG
Tast- oder sichtbare Runzeln und Falten können auftreten, wenn das darüberliegende Gewebe unzureichend oder zu dünn ist, wenig oder kein Unterhautfettgewebe vorhanden ist, Implantate verwendet werden, die für die chirurgisch angelegte Tasche oder die anatomische Struktur der Patientin zu groß sind, und die Plazierung subkutan vorgenommen wird. Eine Faltenbildung kann zur Verdünnung und Erosion des benachbarten Gewebes und zur Extrusion des Implantats führen. Anzeichen von Hautentzündungen wie Berührungsschmerzhaftigkeit und Erytheme können auf eine Verdünnung oder Erosion der Haut hinweisen und müssen umgehend untersucht werden. Tastbare Fältchen bzw. Falten im Ventil können mit tastbaren Tumoren verwechselt werden; in Zweifelsfällen ist daher eine umgehende Untersuchung angezeigt.
GEBRAUCHSANWEISUNG
VERPACKUNG
Das Produkt wird steril in einer versiegelten, doppelten Primärverpackung geliefert. Bei beschädigter oder geöffneter Verpackung ist die Sterilität des Produkts nicht mehr gewährleistet. An der Primärverpackung sind Abreißetiketten mit den Patientendaten angebracht. Nagor empfiehlt, diese Etiketten gegebenenfalls der Patientenakte hinzuzufügen und sie außerdem zu Informationszwecken an die Patienten auszuhändigen.
LAGER- UND TRANSPORTBEDINGUNGEN
Für Brustimplantate mit Gelfüllung gelten keine besonderen Lager- oder Transportbedingungen.
STERILITÄT
Die Brustimplantate werden steril geliefert, nachdem sie in geprüften, streng kontrollierten Sterilisierungszyklen mit Heißluftsterilisation verarbeitet wurden. Die Sterilität wird gemäß den geltenden Standards verifiziert. Die Sterilität des Produkts wird nur bewahrt, wenn die Verpackung intakt und unbeschädigt ist. Das Produkt nicht verwenden, wenn die Verpackung beschädigt oder geöffnet wurde. Vor der Rücksendung des Produkts muss eine Genehmigung angefordert werden.
ÖFFNEN DES VERPACKTEN STERILEN PRODUKTS
- Ziehen Sie die Lasche an der Ecke des äußeren Behälters auf, um die Klappe der äußeren Primärverpackung unter sauberen, aseptischen Bedingungen zu öffnen.
- Entfernen Sie die innere Primärverpackung aus der äußeren Primärverpackung. Dies kann mit einer der folgenden Methoden erfolgen:
a) Der innere Behälter kann über die vertiefte Fläche entfernt werden.
b) Drehen Sie die äußere Primärverpackung über dem sterilen Feld um. Damit kann die versiegelte innere Primärverpackung sanft auf das Feld fallen. - Ziehen Sie die Lasche an der Ecke des inneren Behälters auf, um die Klappe der inneren Primärverpackung zu öffnen.
PRÜFUNG UND HANDHABUNG DES PRODUKTS
- Produkt visuell auf Anzeichen von partikulären Kontaminationen, Beschädigungen und Lecks untersuchen.
- Prothese bis zur Implantation in sterilem Wasser oder normaler Kochsalzlösung aufbewahren, um einen Kontakt mit aerogenen oder im Operationsfeld enthaltenen partikulären Kontaminanzien zu vermeiden.
- Legen sie die Implantate nicht in Lösungen mit Jod oder Betadine ein. Wenn Lösungen mit Jod oder Betadine in den Brusttaschen verwendet werden, so muss sichergestellt werden, dass die Taschen sorgfältig ausgespült werden und keine Restbestände der Lösung in den Taschen verbleiben.
- Gelgefüllte Brustimplantaten können Luftblasen enthalten. Diese entstehen normalerweise während der Sterilisation. Sie haben keine Auswirkung auf die Unversehrtheit oder Leistung des Produkts.
- Verwenden Sie nur fusselfreie Einwegtücher, um sicherzugehen, dass an der Implantatoberfläche keine Partikel verbleiben.
KONTAMINATION DER IMPLANTATE
Die Prothesen müssen sorgfältig gehandhabt werden, um jeden Kontakt mit Oberflächenkontaminanzien wie Talkumpuder, Staub und Hautfett zu vermeiden. Die Prothesen müssen vor der Implantation auf Kontaminationen überprüft werden. Eine Kontamination bei der Operation erhöht das Risiko periprosthetischer Infektionen und möglicherweise von Kapselkontrakturen.
Strukturierte Silikonoberflächen sind potentiell anfälliger für Kontaminationen als glatte Silikonoberflächen. Besondere Sorgfalt ist bei der Handhabung von Implantaten mit strukturierter Oberfläche geboten. Nagor Ltd. übernimmt keine Verantwortung für Kontaminationen durch andere Substanzen, die auftreten, nachdem das Produkt unser Haus verlassen hat.
OBERFLÄCHENKONTAMINANZIEN (TALKUMPUDER, STAUB, FASERN, ÖL) AUF DER OBERFLÄCHE VON IMPLANTATEN KÖNNEN FREMDKÖRPERREAKTIONEN AUSLÖSEN. PROTHESEN NUR MIT OPERATIONSHANDSCHUHEN (VON DENEN DER TALKUMPUDER ABGESPÜLT WURDE) UNTER STRENG ASEPTISCHEN BEDINGUNGEN HANDHABEN. KONTAMINIERTE PRODUKTE NICHT IMPLANTIEREN.
Für den Fall einer Kontamination müssen stets Reserveimplantate bereitgehalten werden.
OPERATIONSVERFAHREN
Die Wahl der korrekten Operationsverfahren und -techniken liegt in der ärztlichen Verantwortung. Der Chirurg muß die Eignung des gewählten Verfahrens anhand aktueller, akzeptabler Techniken, seines persönlichen Urteilsvermögens und seiner Erfahrung beurteilen. Die geeignete Größe und Form der Implantate muß individuell für jede Patientin vom Chirurgen bestimmt werden.
Anmerkung: Die Größe des Brustimplantats kann auf dem Produktetikett entweder als Masse (in Gramm) oder als Volumen (in Millilitern) angegeben sein. Aufgrund der Art des für die Gelfüllung verwendeten Materials kann die Masse als mit dem Volumen identisch angesehen werden.
BESONDERE RICHTLINIEN FÜR DIE VERWENDUNG VON CogelÒ BRUSTIMPLANTATEN
- Die Größe sollte mehr nach der vorhandenen Ausdehnung, den Maßen der Patientin und den individuellen Merkmalen der Brust als nach dem gewünschten Volumen oder Projektionen gewählt werden.
- Die vorgeformten Formen der CoGelÒ Implantate sind viel fester als andere mit Kohäsivgel gefüllte Implantate. Daher sollte der chirurgische Einschnitt größer sein als bei zusammendrückbaren Implantaten.
- Falls notwendig sollte die neue inframammäre Falte gegebenenfalls ca. 1 cm unter der natürlichen Falte liegen.
- Der empfohlene Zugang ist über die inframammäre Falte. Es liegt in der Verantwortung des Chirurgen, zu entscheiden, ob eine axillare oder transareolare Plazierung möglich ist. Wir möchten warnend darauf hinweisen, daß das Einbringen und die Ausrichtung aufgrund der größeren Festigkeit des Gels schwieriger sein kann.
- Submuskuläre Plazierung (eventuell mit unterer Bandfreigabe) sollte soweit möglich vorgezogen werden. Da das Gel hochkohäsiv ist, ist sein Radius am oberen Scheitelrand schärfer ausgebildet. Submuskuläre Plazierung verringert die Wahrscheinlichkeit, daß dieser Scheitelradius fühlbar ist.
- Wenden Sie während der Platzierung von GoGelÒ Implantaten KEINE Gewalt an. Übertriebene Handhabung von CoGelÒ Implantaten kann zu einer permanenten Verformung des kohäsiven Gels und zum Verlust der Implantatform führen.
- Die Beibehaltung der richtigen Ausrichtung und das Verhindern einer Rotation in der postoperativen Phase wird unterstützt durch:
- Das Schaffen einer Prothesentasche, die eng an das Implantat anliegt.
- Das Schaffen einer „trockenen“ Prothesentasche.
- Eine postoperative externe Immobilisierung zur Erlangung der Implantatstabilisation.
- Alle Brustimplantate können sich unter Umständen in der unmittelbaren postoperativen Phase verdrehen. Oben genannte Richtlinien helfen dies bei anatomisch geformten Implantaten zu verhindern.
- Die RICHTIGE AUSRICHTUNG IST bei der Verwendung jedes anatomischen GoGelÒ Implantats SEHR WICHTIG, da die konische Form der Implantate einen Scheitel aufweist. Die richtige Ausrichtung während der Implantation wird durch die folgenden Ausrichtungsmarkierungen unterstützt:
CoGel XA, XM, XL®
- Eine fühlbare Ausrichtungspfeilmarkierung an der Rückseite, im Mittelpunkt über dem unteren Implantatrand. Die Spitze der Pfeilmarkierung ist vertikal positioniert.
- Eine sichtbare röntgenundurchlässige Linienmarkierung verläuft vertikal nach unten durch den Pfeil, an dem unteren Implantatrand vorbei und weiter nach oben auf die Vorderseite. Beide Ausrichtungsmarkierungen helfen bei der korrekten vertikalen Platzierung während der Operation.
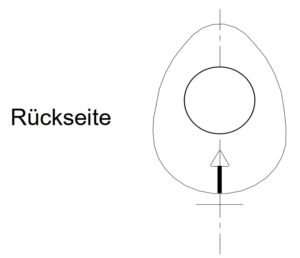
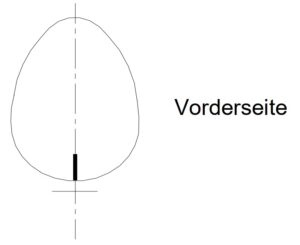
Schematische Darstellung, in der die Ausrichtungsmarkierungen gezeigt werden.CoGel XF1- 3, XM1-3, XL1-3®
-
- Zwei palpable runde Positionierungsmarkierungen befinden sich auf der hinteren Oberfläche des Implantats auf zwölf Uhr im oberen Bereich.
- eine palpable runde Positionierungsmarkierung befindet sich auf der hinteren Oberfläche des Implantats auf 10 und 2 Uhr im oberen Bereich und auf 6 Uhr im unteren Bereich.
- Zwei palpable runde Positionierungsmarkierungen befinden sich auf der vorderen Oberfläche des Implantats auf 6 Uhr im unteren Bereich, wobei die beiden Markierungen direkt
Schematische Darstellung, in der die Ausrichtungsmarkierungen gezeigt werden.
ENTSORGUNG DES PRODUKTS
Für dieses Produkt gelten keine besonderen Entsorgungshinweise. Bei der Entsorgung sollten die üblichen Verfahren des jeweiligen Krankenhauses angewandt werden.
RÜCKGABE
Vor der Rückgabe des Produkts:
- Muß schriftlich eine entsprechende Genehmigung angefordert werden.
- Jedem zurückgesandten Produkt, das mit Körperflüssigkeiten in Kontakt gekommen ist, muß eine Dekontaminationsbescheinigung beiliegen.
- Falls zur sicheren Dekontamination/Sterilisation eine Punktion der Hülle eines versiegelten Produkts erforderlich ist, sollte die Oberfläche des Produkts an der Stelle, an der eine mechanische
Einwirkung stattgefunden hat, mit einem Permanentmarker gekennzeichnet werden und ein entsprechender Vermerk auf der Dekontaminationsbescheinigung eingetragen werden.
GARANTIE
Der Hersteller garantiert, daß diese Produkte mit angemessener Sorgfalt hergestellt wurden, und ersetzt Produkte, die nach Prüfung des Herstellers zum Zeitpunkt des Versands defekt waren. Die Auswahl der Patienten, die Operationstechnik, die postoperative Behandlung und Belastung und die Handhabung der Vorrichtungen liegt vollkommen in der Verantwortung des Kunden. Nagor hat keinen Einfluß auf die Bedingungen, unter denen das Produkt benutzt wird, und kann keine Garantie für Nutzen oder gegen Schäden geben, die durch die Benutzung dieses Produkts entstehen können. Nagor übernimmt keine Haftung für beiläufig entstandene oder Folgeschäden oder Unkosten, die direkt oder indirekt aus der Benutzung dieser Vorrichtung erwachsen. Alle anderen Garantien (auch indirekte bzw. durch Gesetz oder anderweitig bedingte) werden im maximalen dem Gesetz nach zulässigen Umfang ausgeschlossen.
ABGABEBHINWEIS
Nach US-amerikanischer Bundesgesetzgebung darf diese Vorrichtung nur durch einen Arzt oder auf Anweisung eines Arztes verkauft werden.
LITERATUR
Literaturangaben können auf Anfrage von Nagor Ltd bezogen werden.
ERLÄUTERUNGEN
QUANTITY = Anzahl der gelieferten Produkte
5 Ein spätes Serom wird definiert als eine vorherrschende seröse Ansammlung von periprothetischer Flüssigkeit, die ≥1 Jahr nach der Implantation entsteht.
6 Ein frühes Serom wird definiert als eine vorherrschende seröse Ansammlung von periprothetischer Flüssigkeit, die < 1 Jahr nach der Implantation entsteht.